Polymerázová reťazová reakcia (angl. polymerase chain reaction, skratka PCR) je základná metóda molekulárnej biológie, ktorá slúži na amplifikáciu (zmnoženie) molekúl DNA v laboratórnych podmienkach využívajúc enzým DNA-polymerázu a synteticky pripravené oligonukleotidy. Zmnožená molekula DNA sa nazýva PCR produkt alebo amplikón. PCR je exponenciálna reakcia a teoreticky je možné aj z jedinej molekuly DNA vytvoriť ľubovolné množstvo kópií.
Táto metóda bola revolučným objavom Američana KARYHO MULLISA (1944–2019) v roku 1983 (Nobelova cena za chémiu v roku 1993) a dnes je súčasťou mnohých komplexnejších metodík a analýz. Štandardne sa používa v molekulárnej biológii, genetike, mikrobiológii, fyziológii, medicíne ako aj v mnohých iných oblastiach biologického výskumu. Aplikácie PCR sú v mnohých prípadoch rýchlejšou a lacnejšou náhradou klasických molekulárno-biologických metód akými sú klonovanie DNA a northernova hybridizácia.
Čo budeme potrebovať... link
Žiadna DNA-polymeráza nezačne syntézu komplementárneho vlákna DNA bez prekurzoru v podobne krátkeho vlákna DNA alebo RNA. Primer (čítaj 'prajmer') je krátky oligonukleotid, ktorým sa iniciuje replikácia DNA v podmienkach živej bunky ale taktiež aj v laboratórnych podmienkach (in vitro). Primer na základe komplementarity nasadá na vlákno DNA a následne sa predlžuje polymerázou v smere 5'-3'. Často nie je potrebné namnožiť celú molekulu DNA, ale len niektoré jej úseky (napr. gény), takže potreba použiť primer je naopak veľkou výhodou. Do PCR sa preto štandardne pridávajú dva odlišné oligonukleotidy v rovnakej koncentrácii, ktorými sa „označí” ľavý (priamy primer, angl. forward) a pravý koniec (reverzný primer, angl. reverse) amplifikovanej DNA. Dochádza teda k namnoženiu len takých kusov DNA, ktoré sú ohraničené týmito primermi.
Primery do PCR sa syntetizujú na objednávku a cena sa odvíja od ich dĺžky.
Podmienkou replikácie DNA je taktiež jej denaturácia, t.j. oddelenie dvoch vláken dvojvláknovej DNA. K tomu je potrebná vysoká teplota (cca 90–100 °C). Do PCR sa preto pridáva termostabilná rekombinantná Taq-polymeráza (DNA-polymeráza izolovaná z termofilnej baktérie Thermus aquaticus žijúcej v termálnych prameňoch), ktorej optimálna aktivita sa dosahuje pri teplote 72 °C. V súčasnosti existuje viacero druhov rekombinantných Taq-polymeráz a iných (napr. Pfu-polymeráza) dodávaných rôznymi biotechnologickými firmami.
Ľudská DNA-polymeráza δ (delta) replikuje DNA pri teplote ľudského tela (t.j. cca 36,8 °C) a denaturácia DNA sa zabezpečuje v bunkách enzymaticky (DNA-helikáza). Baktéria Thermus aquaticus bola prvýkrát objavená v roku 1969 v Yellowstonskom národnom parku. Neprežije pri teplote nižšej ako 55 °C, naopak vydrží aj dlhodobé teploty >80 °C.
K syntéze nových molekúl DNA sú samozrejme potrebné „stavebné čiastočky” v podobe deoxyribonukleozidtrifosfátov, alebo skrátene dNTP. Pomer všetkých štyroch zložiek (dATP, dCTP, dTTP a dGTP) musí byť rovnaký, aby nedochádzalo k chybám pri replikácii. Okrem toho každá DNA-polymeráza vyžaduje ako kofaktor pri polymerizácii horečnaté katióny (Mg²⁺) a v podmienkach in vitro aj vlastný tlmivý roztok (pufor), pri použití ktorého má optimálnu aktivitu a stabilitu.
DNA-polymeráza, primery, horčík, pufor a dNTP sa riedia v sterilnej destilovanej vode, výsledkom čoho je tzv. mastermix. PCR je veľmi citlivá na kontamináciu, a preto sa pri príprave roztoku mastermixu vyžaduje veľmi precízna a sterilná práca, takže sa pracuje za tzv. „DNA-free” podmienok. Napokon sa do mastermixu pridáva vzorka DNA, ktorú chceme (resp. jej časť) amplifikovať. Nazýva sa aj templátová DNA (templát). Takto pripravená PCR reakčná zmes v mikroskúmavke sa vkladá do samotného prístroja na PCR reakciu, ktorý sa nazýva termálny cyklér alebo len cyklér.
| zložka | koncentrácia | objem do 25 µl reakčnej zmesi |
| PCR pufor + MgCl₂ | 10x + 15 mM | 2,5 µl |
| dNTP | 10 mM | 0,5 µl |
| primer (priamy + reverzný) | 12,5 µM | 0,5 µl + 0,5 µl |
| Taq-polymeráza | 5 U/µl | 0,2 µl |
| DNA templát | 10 ng/µl | 1 µl |
| deionizovaná sterilná voda | - | 19,8 µl |
Priebeh PCR link
Amplifikácia DNA metódou PCR sa uskutočňuje cyklickým procesom, pričom každý cyklus pozostáva z troch základných krokov:
Denaturácia – tepelná denaturácia templátovej DNA zohriatím reakčnej zmesi na teplotu >90 °C.
Anelácia – za poklesu teploty na cca 45–65 °C (závisí od dĺžky a sekvencie primerov, najmä množstva G–C párov) nastáva hybridizácia primerov s templátovou DNA na komplementárnych miestach.
Poznámka: K úspešnej amplifikácii DNA je potrebné, aby vzdialenosť medzi priamym a reverzným primerom bola dostačujúca (štandardne 100–1 500 bp) z hľadiska času potrebného na polymerizáciu (príliš dlhé alebo naopak príliš krátke fragmenty sa nedajú amplifikovať).Polymerizácia – zvýšením teploty na 72 °C začína Taq-polymeráza syntetizovať komplementárne vlákno DNA z voľných dNTP.
Tieto tri kroky sa cyklicky opakujú v už spomínanom termálnom cykléri 20 až 40-krát a výsledkom je vznik mnohých kópií fragmentu DNA ohraničeného použitými primermi. Množstvo PCR produktu v jednej reakcii môže dosiahnuť hodnoty 0,2–1 µg DNA, čo postačuje na analýzu štandardnými metódami molekulárnej biológie ako je napr. elektroforéza v agarózovom géli.
- Záverečná polymerizácia – tento voliteľný krok prebehne počas PCR len raz, a to na konci PCR programu. Slúži na „dobehnutie” všetkých polymerizačných reakcií, ktoré ešte prebiehajú.
| teplota [T] | čas [t] | počet cyklov | |
| denaturácia | 94 °C | 1 min | 30x |
| anelácia primerov | 58 °C | 1 min | 30x |
| polymerizácia | 72 °C | 1 min | 30x |
| záverečná polymerizácia | 72 °C | 5 min | 1x |
Faktory ovplyvňujúce priebeh PCR link
PCR je možné charakterizovať pomocou nasledovných parametrov:
špecificita – schopnosť amplifikovať len úseky s presnou komplementaritou sekvencií v oblasti primerov. Nižšie anelačné teploty a vyššia koncentrácia Mg²⁺ spravidla špecificitu znižujú, takže dochádza k amplifikácii tzv. nešpecifických fragmentov, ktoré nie sú z cieľovej oblasti, ktorá nás zaujíma.
citlivosť – udáva množstvo templátu, ktoré je možné úspešne amplifikovať za použitých podmienok. Teoreticky možno amplifikovať aj jednu jedinú molekulu DNA, prakticky je to číslo vyššie, takže citlivosť je nižšia.
efektívnosť – aké množstvo molekúl templátu sa kopíruje v jednom cykle. Teoreticky sa kopírujú všetky molekuly, prakticky je toto množstvo nižšie.
fidelita – miera presnosti sekvencie PCR produktu v porovnaní s templátom, t.j. do akej miery je výsledný PCR produkt (DNA fragment) sekvenčne identický s „originálom” – pôvodným templátom. Závisí hlavne od chybovosti enzýmu Taq-polymerázy a pomeru jednotlivých dNTP. Je nepriamo úmerná počtu zle inkorporovaných – mutovaných nukleotidov.
Pri miešaní mastermixu treba dbať na to, aby zmes neobsahovala príliš veľa inhibítorov PCR, predovšetkým aktivity polymerázy. K nim patria najmä detergenty, organické rozpúšťadlá, proteázy, nukleázy a nadbytok RNA. Všetky tieto zlúčeniny môžu ostať prítomné po izolácii a purifikácii DNA. Mnohé zložky takéhoto mastermixu ovplyvňujú aj koncentráciu horečnatých iónov (napr. EDTA ako hlavná zložka „uskladňovacieho” roztoku pre čistú naizolovanú DNA), ktorú treba podľa potreby zvýšiť.
Pozitívna a negatívna kontrola PCR link
Keď potrebujeme identifikovať prítomnosť templátu (napr. vírusovej DNA) v nejakej neznámej zmesi nukleových kyselín, spravidla robíme jednu extra PCR reakciu, kde ako templát použijeme dostatočné množstvo známej DNA, na ktorej s určitosťou prebehne amplifikácia špecifického produktu, ktorý chceme dokázať aj v neznámych vzorkách. Pozitívna kontrola je teda taká vzorka, "ako to má vyzerať". V prípade, že nedôjde k amplifikácii DNA v pozitívnej kontrole, nemôžeme sa s určitosťou spoľahnúť na výsledok ostatných reakcií (napr. keď výjdu všetky vzorky negatívne).
Pojem negatívna kontrola zahŕňa nadbytočnú PCR, ktorá obsahuje všetky reagencie mastermixu, okrem templátovej DNA. Prípadná amplifikácia DNA fragmentov v tejto vzorke poukazuje na kontamináciu, t.j. prítomnosť neželanej DNA v niektorej zo zložiek PCR (kontaminované pufre, dNTP-čka, primery, voda) alebo nesterilné pipetovanie reagencií počas prípravy mastermixu. Negatívna kontrola je dôležitá hlavne pri diagnostických PCR, kde prítomnosť DNA fragmentov v negatívnej kontrole spôsobuje nedôveryhodnosť pozitívnej reakcie aj u reakcií s prítomnou testovanou vzorkou DNA. V takýchto prípadoch je často posledným riešením výmena všetkých zložiek (primery, dNTP, pufor, horčík, voda) a sprísnenie práce (sterilné rukavice, dekontaminovaný odev) za účelom zachovania sterilných "DNA-free" podmienok.
Návrh primerov link
Primery sú krátke oligonukleotidy, ktoré sa navrhujú ako primerový pár − priamy a reverzný primer. Teplota topenia \( (T_m) \) je hraničná teplota, pri ktorej je ½ primerov prítomná v jednovláknovej forme a druhá ½ je hybridizovaná k DNA. Anelačná teplota je cca o 4–5 °C nižšia ako \( T_m \), čím sa zvyšuje podiel primerov hybridizovaných s denaturovanou DNA počas anelačného kroku PCR.
Pri návrhu primerov treba dbať na určité pravidlá:
- ideálna teplota topenia je v rozmedzí 50–60 °C, pričom v rámci navrhovaného páru by nemal byť rozdiel väčší ako 5 °C
- ideálna dĺžka pre väčšina aplikácií je 16–25 nukleotidov
- doporučená hodnota obsahu G-C párov je v rozmedzí 40–60 %
- rovnomerné rozmiestnenie nukleotidov (tzn. nemali by byť 4 rovnaké nukleotidy za sebou)
- sekvencia primerov musí byť jedinečná, aby nasadali len na špecifické miesto na templátovej DNA, pričom špecificita primeru je ovplyvnená predovšetkým sekvenciou na 3'-konci (na 5'-konci môže obsahovať nekomplementárne sekvencie)
- do mastermixu pridávať primery v rovnakej koncentrácii
- predchádzať vzniku komplementárnych úsekov v rámci jedného primeru (tvorba sekundárnych štruktúr, vláseniek, tzv. self-complementarity) a medzi primermi (ak pri párovaní priameho a reverzného primeru zostáva voľný 3'-koniec, dochádza k syntéze krátkych nešpecifických produktov tzv. primer dimérov, ktoré znižujú účinnosť PCR)
Teplotu topenia \( (T_m) \) primerov možno vypočítať podľa vzorca:
\( T_m = 4 \times (počet[C] + počet[G]) + 2 \times (počet[A] + počet[T]) \)
Takáto teplota topenia sa označuje ako základná teplota topenia (angl. basic \( T_m \)) a považuje sa za najmenej presnú, avšak najčastejšie používanú v praxi. Určitú formu korekcie predstavuje tzv. salt-adjusted \( T_m \) a ešte presnejší model tzv. nearest neighbour \( T_m \), ktorých názov nemá mne známy slovenský ekvivalent. Akú teplotu teda zvoliť? V princípe tú, ktorá vám je sympatickejšia, pretože aj tak je teplota topenia len „prvý nástrel”, ktorý treba optimalizovať s ohľadom na ostatné parametre (koncentrácie komponentov, časy) a konkrétnu aplikáciu. PCR ovplyvňujú negatívne najviac fenomény self-complementarity a primer diméry.
Bioinformatické programy link
Bioinformatika je interdisciplinárna veda, spojenie biológie s informatikou. Neustálym rozvojom metód molekulárnej biológie, ako aj pribúdaním nových sekvencií DNA, RNA a proteínov, zvyšujú sa nároky na uchovávanie, triedenie a analýzu biologických dát pomocou počítača. Hlavnou úlohou bioinformatiky je vývoj programov (softvéru) pracujúcich s biologickými údajmi. Jedným z takých bioinformatických programov je aj softvér na návrh primerov.
Návrh (dizajn) primerov pre bežné diagnostické potreby už v súčasnosti nie je žiadny problém. Pre samotný návrh primerov sa mi osvedčila stránka amerického ministerstva zdravotnícva (NCBI − National Center for Biotechnology Information), ktorá, okrem iného, ponúka množstvo ďalších užitočných nástrojov, databázu nukleových kyselín a bielkovín. Pomocou bioinformatického softvéru je možné dizajnovať niekoľko primerových párov súčasne, ktoré sú vhodné aj pre niektoré dolespomenuté variácie PCR (napr. multiplex PCR, nested PCR, alelovo-špecifická PCR a pod.).
Ak by ste si chceli otestovať základné vlastnosti primerov, ako je napr. teplota topenia za rôzneho zloženia reakčného pufru (koncentrácia horčíka a pod.), tvorba vnútorných vláseniek alebo primer dimérov, môžete využiť softvér OligoAnalyzer od firmy IDT − Integrated DNA Technologies, ktorá sa zaoberá syntézou primerov. Použitie programu je bezplatné.
Variácie PCR link
Jedná sa o všetky modifikácie PCR protokolu, tzn. zloženia reakčnej zmesi a nastavenia PCR programu, ktoré sú pre konkrétne účely lepšie ako štandardná PCR popísaná vyššie. Z tých mnohých, ktoré existujú, vyberiem tie, ktoré pokladám za dôležité:
hot-start PCR – reakcia využívajúca rekombinantný enzým Taq-polymerázy, ktorý na iniciáciu polymerizácie vyžaduje vysokú aktivačnú teplotu (napr. 95 °C, 5 min) pred záhajením 1. cyklu – bežná Taq-polymeráza má nízku aktivitu aj počas pipetovania mastermixu, kedy navyše funguje veľmi nepresne, hot-start polymeráza je naopak úplne neaktívna, takže jej použitie zvyšuje špecificitu a fidelitu PCR reakcie
touchdown PCR – počiatočné cykly majú vysokú anelačnú teplotu, ktorá sa postupne v ďalších cykloch znižuje – vysoká teplota zabráni nešpecifickým väzbám primerov s templátovou DNA a neskoršia nižšia teplota namnoží už len špecifické PCR produkty
nested PCR – dvojkroková PCR; 1. krok: amplifikuje sa dlhší DNA fragment pomocou jednej sady primerov; 2. krok: druhá sada primerov amplifikuje špecifický vnútorný (kratší) DNA fragment, pričom ako templát je použitá vzorka z 1. PCR – zvyšuje sa špecifickosť a citlivosť diagnostických PCR
multiplex PCR – v jednej reakčnej zmesi je viac primerových párov, takže prebieha amplifikácia viacerých úsekov DNA v rovnakom čase – urýchľuje celkový čas analýzy a znižuje celkové použité financie, vyžaduje však dôsledný dizajn primerov
real-time PCR (kvantitatívna PCR) – po každom cykle sa meria množstvo DNA na základe fluorescencie – zistenie presného množstva pôvodnej templátovej DNA vo vzorke (absolútna kvantifikácia) alebo porovnanie množstva DNA vzhľadom na inú vzorku (relatívna kvantifikácia)
RT-PCR – dvojkroková procedúra na amplifikáciu PCR produktu z izolovanej mRNA; 1. krok: mRNA sa prepíše reverznou transkriptázou do jednovláknovej komplementárnej DNA (cDNA); 2. krok: nasleduje štandardná PCR na amplifikáciu DNA - detekcia génovej expresie
alelovo-špecifická PCR – použijú sa primery s odlišnou sekvenciou na 3'-koncoch a maximálna špecificita PCR; reakcia neprebehne, ak miesto na templátovej DNA nie je komplementárne k 3'-koncu primeru (t.j. je mutované) – detekcia konkrétnych mutácií v prípade genetických ochorení
mutagenéza prostredníctvom PCR – na amplifikáciu sa používajú dlhé primery, ktoré majú cielene mutovaný(é) nukleotid(y) v strednej časti – mutácia v strede primeru neovplyvní aneláciu s templátovou DNA, pričom výsledkom je tvorba PCR produktu s cielenou mutovanou sekvenciou DNA
Aplikácie PCR link
Metóda PCR sa využíva v mnohých oblastiach. Podľa účelu použitia sa prispôsobujú konkrétne podmienky.
Základnou aplikáciou je detekcia prítomnosti špecifického úseku (ohraničeného primermi) v zmesi DNA (analytická PCR, diagnostická PCR). Táto metóda sa využíva v medicíne napríklad na detekciu mutácií spôsobujúcich genetické ochorenia, na dôkaz prítomnosti patogénnych alebo nekultivovateľných mikroorganizmov a vírusov, v onkológii na sledovanie markerov nádorových ochorení. Analogicky v poľnohospodárstve sa PCR používa na sledovanie vlastností hospodárskych zvierat a plodín a pod. V kriminalistike sa táto metóda používa na stanovenie identity osôb (angl. DNA profiling, DNA typing, DNA fingerprinting) a je náhradou relatívne zdĺhavej a drahej southernovej hybridizácie.
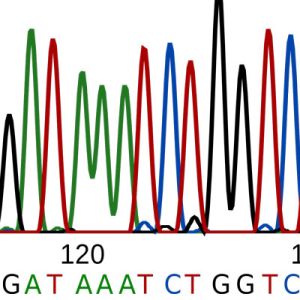
V niektorých prípadoch je potrebné okrem zistenia prítomnosti špecifickej molekuly DNA zistiť aj rozdiely vo vnútornej sekvencii PCR produktov v odlišných vzorkách. V tomto prípade sa produkty analyzujú sekvenovaním DNA, restrikčným štiepením alebo hybridizáciou. Takto je možné rozlíšiť mutovanú a pôvodnú alelu génu (napr. pri genetických ochoreniach) a rôzne varianty patogénov (napr. vírusov).
Druhou aplikáciou PCR je príprava špecifickej DNA, ktorá sa použije na tvorbu rekombinantnej DNA (preparatívna PCR). Upravený PCR produkt je možné využiť napríklad na produkciu rekombinantných proteínov, a to na výskumné alebo komerčné účely.